F Rubba, S Campanile, C Viscardi, P Riccio, A Carnimeo, A Bosco, CM Mendillo , E Cascone, R Montalti, P Montuori , E Bianco R Troisi
“Mi ha sentito? Un ospedale senza fornitura d’acqua, il reparto delle puerpere vicino a quello delle malattie infettive. Ho rifiutato di lavorare per l’inferno” W Marasco- Di spalle a questo mondo , 2025
Il presente lavoro nasce dall’esigenza di osservare il blocco operatorio non soltanto come luogo tecnico dell’atto chirurgico, ma come sistema dinamico di relazioni, attraversato da flussi, interazioni e vulnerabilità invisibili che incidono direttamente sulla sicurezza del paziente. L’obiettivo principale è stato quello di analizzare, sotto il profilo organizzativo e strutturale, i percorsi interni al blocco operatorio, con particolare attenzione alla prevenzione delle infezioni correlate all’assistenza (ICA) nel paziente sottoposto a trapianto renale, soggetto che per definizione presenta una condizione di elevata fragilità immunologica [1,11]. Lo studio si articola in due dimensioni complementari:
- La componente osservazionale si è basata su un’analisi descrittiva dell’organizzazione degli spazi, dei percorsi assistenziali e dei flussi di pazienti, operatori e materiali. Tale analisi è stata condotta attraverso lo studio sistematico delle planimetrie e della documentazione organizzativa e normativa disponibile [6], consentendo di ricostruire la struttura teorica dei percorsi e di confrontarla con l’assetto reale;
- La componente sperimentale, di natura non interventistica, ha invece riguardato l’identificazione delle interferenze critiche tra i flussi e l’elaborazione di proposte di miglioramento organizzativo e procedurale. L’obiettivo non è stato quello di modificare l’assetto architettonico esistente, bensì di individuare misure compensative coerenti con la normativa vigente e con le buone pratiche in materia di prevenzione del rischio infettivo [1,4].
Questo approccio integrato ha permesso di coniugare l’osservazione sistematica del contesto reale con una riflessione applicativa orientata al miglioramento continuo, rafforzando la prospettiva della governance della sicurezza e promuovendo un modello organizzativo fondato sull’analisi critica dei processi e sull’ottimizzazione dei percorsi assistenziali [16].
Lo studio è stato condotto presso il blocco operatorio dell’Azienda Ospedaliera Universitaria Federico II, con riferimento specifico alla Piastra B dell’Edificio 5, area dedicata all’attività trapiantologica. La Piastra B si inserisce in un contesto di edilizia sanitaria complessa, caratterizzato dalla coesistenza di sale operatorie, aree filtro, locali di supporto, spazi amministrativi e corridoi di collegamento [15]. In tale configurazione convergono e si sovrappongono molteplici tipologie di flussi: clinici, logistici, assistenziali.
All’interno del blocco operatorio si riscontra inoltre la presenza di due distinte tipologie di pazienti: da un lato il paziente candidato a trapianto o già sottoposto a trapianto renale; dall’altro il paziente dialitico che, per esigenze organizzative e logistiche, viene indirizzato ad effettuare il trattamento all’interno del medesimo blocco. Tale coesistenza determina una criticità gestionale rilevante, in quanto entrambe le categorie condividono percorsi e flussi comuni. La condizione di immunodepressione che contraddistingue il paziente trapiantato conferisce a questo contesto una rilevanza particolare sotto il profilo del rischio di ICA [1,10,11]. La condivisione degli stessi corridoi e delle medesime aree di transito con pazienti dializzati può favorire l’insorgenza di problematiche correlate alla gestione delle infezioni crociate, soprattutto nella fase post-trapianto [3]. In tale scenario, ogni interferenza tra percorsi e ogni possibile contaminazione indiretta assumono un peso amplificato rispetto ad altri setting assistenziali, rendendo imprescindibile un’attenta regolamentazione organizzativa dei flussi [8].
L’analisi è stata sviluppata attraverso tre strumenti principali:
· studio delle planimetrie del blocco operatorio e della Piastra B;
· analisi della documentazione normativa e organizzativa;
· mappatura sistematica dei flussi interni.
Sono stati individuati cinque flussi principali:
· flusso del paziente sottoposto a trapianto d’organo;
· flusso del paziente sottoposto a dialisi;
· flusso del personale sanitario;
· flusso dei materiali puliti;
· flusso dei materiali sporchi.
La valutazione del rischio infettivo è stata sviluppata attraverso un’analisi sistematica fondata su criteri strutturati e coerenti con i principi della prevenzione del rischio biologico [8]. In particolare, l’attenzione si è concentrata sulla tipologia dei flussi coinvolti, sulla frequenza e sulle modalità concrete di utilizzo dei percorsi, nonché sulla presenza di possibili interferenze tra flussi puliti e sporchi. È stata inoltre considerata la probabilità di contaminazione crociata, valutando in che misura la condivisione degli spazi potesse favorire il trasferimento indiretto di microrganismi attraverso superfici, presidi, aria o contatti occasionali mediati dal personale sanitario [13]. Un ulteriore elemento di analisi ha riguardato la presenza o l’assenza di misure di attenuazione del rischio, quali zone filtro, separazioni strutturali o specifiche procedure organizzative [14]. Le criticità emerse sono state quindi ponderate e classificate in relazione al loro potenziale impatto sul rischio infettivo, non in termini astratti, ma in rapporto alla vulnerabilità del paziente e alla concreta operatività del contesto [1,11]. Tale classificazione ha costituito la base per l’elaborazione di proposte migliorative mirate. Laddove l’intervento strutturale non risultasse praticabile, si è privilegiato un approccio di tipo organizzativo e procedurale, valorizzando in particolare la separazione temporale dei flussi quale misura compensativa capace di ridurre le interferenze e di rafforzare la sicurezza dei percorsi assistenziali senza modificare l’assetto architettonico esistente [14].
La planimetria della Piastra B restituisce l’immagine di un organismo architettonico complesso, nel quale ogni spazio risponde a una funzione e ogni percorso traduce un principio organizzativo. La struttura si sviluppa lungo direttrici di percorrenza chiaramente definite, che organizzano e collegano due macro-aree funzionalmente distinte ma integrate in un unico sistema. L’impianto distributivo non è casuale, bensì risponde a una logica progettuale volta a garantire ordine, separazione dei percorsi e coerenza tra funzione e spazio:
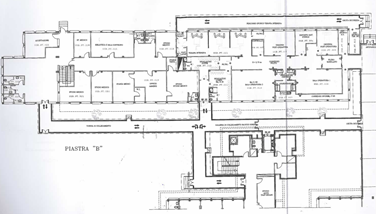
- Nella porzione sinistra della planimetria si colloca l’area di supporto e amministrativa: studi medici, biblioteca, sala convegni, uffici e accettazione delineano uno spazio dedicato alle attività di programmazione, confronto e gestione. Si tratta di ambienti caratterizzati da una bassa carica batterica, fisicamente separati dall’area chirurgica, concepiti per consentire al personale di svolgere funzioni organizzative e scientifiche senza interferire con le attività cliniche ad alta intensità assistenziale.
- Nella porzione destra si concentra invece il nucleo operativo del blocco: le sale operatorie, protette da zone filtro che regolano l’accesso e garantiscono la decontaminazione, l’area di terapia intensiva e la degenza post-operatoria. Qui lo spazio assume una dimensione eminentemente clinica, pensata per accogliere il paziente nelle fasi più critiche del percorso assistenziale. La contiguità funzionale tra questi ambienti non è soltanto un elemento architettonico, ma una scelta organizzativa precisa: ridurre al minimo i tempi di trasferimento del paziente critico, assicurare continuità assistenziale e mantenere condizioni di massima sterilità lungo tutto il tragitto intraospedaliero.
La mappatura cromatica ha permesso di distinguere chiaramente i percorsi.
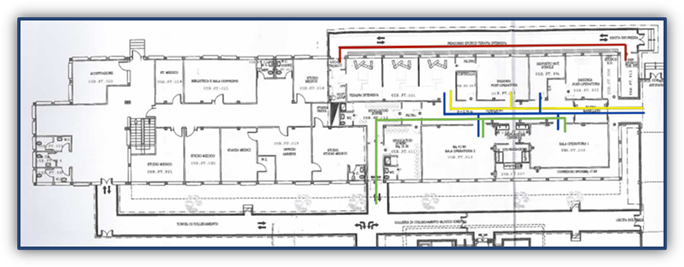
Il percorso sporco (linea rossa) si sviluppa lungo un corridoio perimetrale esterno, separato dalle aree sterili. Esso garantisce l’evacuazione di rifiuti biologici, biancheria infetta e strumentazione da sterilizzare, nel rispetto del principio della “marcia in avanti”.
Il percorso pulito degli operatori (linea verde) prevede il passaggio obbligato attraverso zone filtro, spogliatoi e aree di lavaggio chirurgico, assicurando che solo personale adeguatamente decontaminato acceda alle aree critiche.
I percorsi dei pazienti si distinguono in:
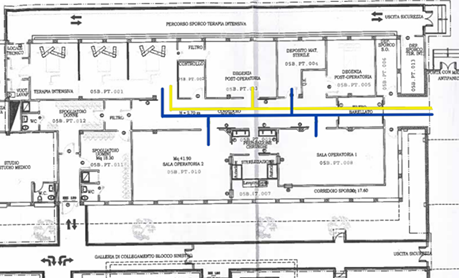
· percorso del paziente trapiantato (linea blu), diretto verso la sala operatoria con massimo livello di protezione;
· percorso del paziente dializzato (linea gialla), che si dirige verso terapia intensiva e aree nefrologiche di supporto.
L’analisi dei percorsi ha portato alla luce una criticità strutturale di particolare rilievo: la sovrapposizione tra il tragitto destinato al paziente sottoposto a trapianto e quello riservato al paziente dializzato. Entrambi i flussi prendono avvio dalla medesima zona filtro e proseguono lungo lo stesso corridoio di distribuzione, determinando una continuità spaziale che annulla, di fatto, la distinzione tra percorsi assistenziali profondamente diversi per natura e livello di vulnerabilità. Questa configurazione interrompe il principio fondamentale della separazione dei flussi, cardine dell’organizzazione dei blocchi operatori ad alta complessità. La condivisione degli spazi, in un contesto in cui il controllo della contaminazione rappresenta una priorità assoluta, introduce un elemento di fragilità sistemica. Il paziente trapiantato, soprattutto nella fase perioperatoria, si trova in una condizione di marcata immunodepressione, che lo rende particolarmente suscettibile anche a minime esposizioni ambientali. Parallelamente, il paziente dializzato costituisce una popolazione clinicamente complessa, frequentemente portatrice di accessi vascolari permanenti e, non di rado, di infezioni croniche o colonizzazioni batteriche. La compresenza di tali condizioni lungo il medesimo corridoio amplifica il rischio di contaminazione indiretta, che può realizzarsi attraverso superfici, micro-particelle aerodisperse, presidi sanitari o contatti occasionali mediati dal personale. Ne emerge un evidente disallineamento tra l’assetto strutturale degli spazi e le esigenze clinico-assistenziali proprie del percorso trapiantologico: una discrepanza che non si limita a un dato architettonico, ma si traduce in una vulnerabilità organizzativa con potenziali ricadute sulla sicurezza del paziente più fragile.
Le proposte di miglioramento e le misure compensative elaborate nel presente studio nascono dalla consapevolezza dell’impossibilità di intervenire in modo strutturale sull’architettura esistente. Tale vincolo ha imposto una riflessione orientata verso soluzioni di natura organizzativa e procedurale, capaci di agire non sulla configurazione fisica degli spazi, ma sulle modalità con cui essi vengono quotidianamente utilizzati. In un contesto edilizio complesso e non modificabile, la sicurezza non può essere affidata alla trasformazione materiale dell’ambiente, bensì alla capacità dell’organizzazione di ripensare i propri processi, ridefinire le priorità operative e introdurre strumenti compensativi idonei a mitigare le criticità emerse dall’analisi dei flussi. Tra le proposte figurano:
- Segnaletica orizzontale: un ruolo significativo è attribuito al potenziamento della segnaletica orizzontale. L’introduzione di una codifica cromatica ad alto contrasto, applicata direttamente alla pavimentazione, consentirebbe di creare vere e proprie “corsie di marcia”, immediatamente riconoscibili anche in condizioni di urgenza o elevata pressione assistenziale. Tale soluzione, semplice ma strategica, favorisce il rispetto intuitivo dei percorsi assegnati e contribuisce a ridurre le interferenze accidentali tra flussi a differente livello di rischio, rafforzando la leggibilità organizzativa degli spazi;

- Check-list dedicata all’Igiene dei Flussi: Un ulteriore intervento riguarda l’integrazione delle attuali check-list di sala operatoria con una sezione specificamente dedicata all’igiene dei flussi. Questa integrazione avrebbe la funzione di monitorare in modo sistematico la libertà di transito dei corridoi, il corretto posizionamento di materiali e carrelli e il rispetto delle aree destinate alla logistica. L’obiettivo non è soltanto quello di controllare, ma di promuovere una maggiore consapevolezza organizzativa: rendere visibili le criticità quotidiane, spesso percepite come marginali, e trasformarle in elementi oggetto di verifica strutturata. In tal modo, il controllo delle interferenze logistiche diventa parte integrante della prevenzione delle infezioni correlate all’assistenza;

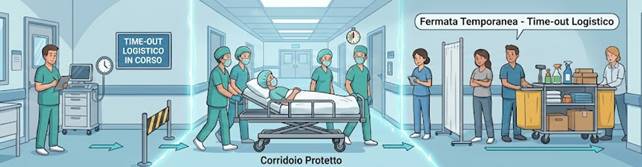
- Protocollo di “Corridoio Protetto”: In relazione al trasporto del paziente trapiantato, si propone l’adozione di un protocollo definito di “corridoio protetto”. La procedura prevede l’attivazione di un breve “time-out logistico”, durante il quale viene temporaneamente sospeso il transito di materiali e di pazienti non trapiantati lungo il percorso interessato. Questa misura introduce una separazione temporale dei flussi che, pur in assenza di un isolamento strutturale dedicato, consente di ridurre l’esposizione del paziente immunodepresso a potenziali fonti di contaminazione. Si tratta di un intervento a costo organizzativo minimo, ma ad alto valore preventivo, capace di trasformare un limite strutturale in un’occasione di regolazione consapevole dei tempi assistenziali;
- Monitoraggio Microclimatico Mirato: si propone l’estensione del monitoraggio ambientale ai punti critici dei corridoi e delle aree di intersezione tra flussi. L’incremento dei campionamenti particellari e microbiologici, con particolare attenzione alle possibili alterazioni dei flussi d’aria, consentirebbe di intercettare precocemente eventuali situazioni di rischio non immediatamente percepibili. In questo modo, la sorveglianza microclimatica non resterebbe confinata alle sole sale operatorie, ma si estenderebbe ai percorsi che traducono fisicamente il PDTA, riconoscendo che anche gli spazi di transito rappresentano ambienti sensibili nella tutela del paziente fragile.
In conclusione, il lavoro ha evidenziato come la prevenzione del rischio infettivo nel paziente trapiantato non possa essere confinata alla dimensione strettamente clinica, ma debba includere l’organizzazione degli spazi, la gestione dei tempi, la logistica e la cultura della sicurezza. Il PDTA non rappresenta soltanto uno strumento di appropriatezza terapeutica, ma una cornice sistemica entro cui collocare la prevenzione lungo tutte le fasi del percorso assistenziale [17]. Nel blocco operatorio, il percorso assistenziale diventa percorso fisico: corridoi, filtri, incroci, spostamenti. Ogni interferenza non governata si traduce in vulnerabilità. Lo studio dimostra che, anche in presenza di vincoli strutturali non modificabili, è possibile intervenire efficacemente attraverso misure organizzative sostenibili. Il contributo offerto da questo lavoro, pur circoscritto a un contesto specifico, propone un modello di analisi replicabile, fondato sull’integrazione tra lettura critica dei percorsi assistenziali e gestione consapevole dei flussi logistici, nella prospettiva di una sicurezza realmente sistemica.
Bibliografia
1. World Health Organization. Global guidelines for the prevention of surgical site infection. Geneva: WHO; 2016.
2. World Health Organization. Guidelines on core components of infection prevention and control programmes. Geneva: WHO; 2016.
3. European Centre for Disease Prevention and Control. Healthcare-associated infections: surgical site infections. Annual epidemiological report. Stockholm: ECDC; 2022.
4. Centers for Disease Control and Prevention. Guideline for the prevention of surgical site infection. Atlanta: CDC; 2017.
5. Ministero della Salute. Piano Nazionale di Contrasto dell’Antimicrobico-Resistenza (PNCAR) 2022–2025. Roma; 2022.
6. Ministero della Salute. Manuale di formazione per il governo clinico: la sicurezza dei pazienti e degli operatori. Roma; 2012.
7. Ministero della Salute. Raccomandazione n. 9: prevenzione delle infezioni del sito chirurgico. Roma; 2008.
8. Società Italiana di Igiene, Medicina Preventiva e Sanità Pubblica. Linee guida per la prevenzione delle infezioni correlate all’assistenza. Roma: SItI; 2019.
9. Istituto Superiore di Sanità. Prevenzione e controllo delle infezioni correlate all’assistenza. Roma: ISS; 2018.
10. European Society for Organ Transplantation. Guidelines for infection management in solid organ transplant recipients. Transplant International. 2019.
11. Fishman JA. Infection in solid-organ transplant recipients. New England Journal of Medicine. 2007;357(25):2601-2614.
12. Mangram AJ, Horan TC, Pearson ML, Silver LC, Jarvis WR. Guideline for prevention of surgical site infection. Infection Control and Hospital Epidemiology. 1999;20(4):250-278.
13. Allegranzi B, Pittet D. Role of hand hygiene in healthcare-associated infection prevention. Journal of Hospital Infection. 2009;73(4):305-315.
14. Associazione Nazionale Medici Direzioni Ospedaliere. Organizzazione e gestione del blocco operatorio. Roma: ANMDO; 2017.
15. Ulrich RS, Zimring C, Zhu X et al. A review of the research literature on evidence-based healthcare design. Health Environments Research & Design Journal. 2008.
16. Joint Commission International. International Patient Safety Goals. Oakbrook Terrace; 2021.
17. Ministero della Salute. Percorsi Diagnostico Terapeutici Assistenziali (PDTA): metodologia e strumenti per l’implementazione. Roma: Ministero della Salute; 2017.




