Il SISTEMA QUALITÀ nei centri di Procreazione Medicalmente Assistita (PMA) ha lo scopo di garantire la sicurezza, l’efficacia e la tracciabilità dei trattamenti. Questi sistemi si basano su normative specifiche e standard internazionali o nazionali, come ad esempio:
Normative di riferimento
- Direttiva Europea 2004/23/CE e successive modifiche: regola la qualità e la sicurezza nella donazione, approvvigionamento, test, lavorazione, conservazione, stoccaggio e distribuzione di cellule e tessuti umani.
- Legge 40/2004 (Italia): disciplina le tecniche di PMA e stabilisce criteri e limiti.
- Linee guida del Centro Nazionale Trapianti (CNT) e del Registro Nazionale PMA (ISS): danno indicazioni operative.
I centri PMA devono adottare un Sistema di Gestione della Qualità (SGQ) secondo standard come:
- ISO 9001:2015 – Questa certificazione attesta che il centro ha un sistema di gestione della qualità che soddisfa determinati standard internazionali. È la norma più generale per la qualità, ma applicabile anche ai centri PMA.
- ISO 15189:2012 – Questa certificazione è specifica per i laboratori medici, inclusi i laboratori di embriologia nei centri PMA. Garantisce che il laboratorio segua gli standard di qualità e sicurezza nelle pratiche diagnostiche e terapeutiche.
- ISO 13485:2016 – Questa certificazione riguarda i dispositivi medici, che sono utilizzati nei trattamenti di PMA (ad esempio, strumenti per la fecondazione in vitro, incubatori, dispositivi per la crioconservazione, etc.). Garantisce che il centro rispetti rigorosi standard di qualità per i dispositivi utilizzati.
- Good Manufacturing Practices (GMP): buone pratiche per la lavorazione di gameti ed embrioni, in particolare nei laboratori di embriologia.


Gli elementi chiave del sistema qualità PMA sono:
- Documentazione e tracciabilità: ogni fase del processo deve essere registrata.
- Gestione del rischio e non conformità.
- Controllo ambientale: monitoraggio della qualità dell’aria e delle superfici nei laboratori.
- Validazione dei processi: tecniche di congelamento, fecondazione, coltura embrionale.
- Formazione continua del personale.
- Audit interni ed esterni.
Accreditamento e certificazione
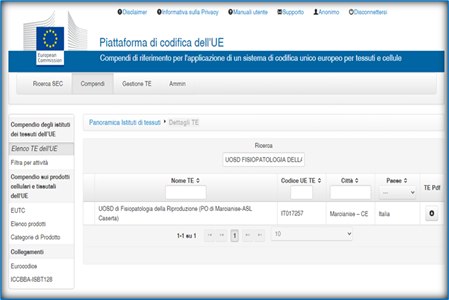

In Italia, i centri PMA devono essere autorizzati e accreditati a livello regionale e registrati presso l’Istituto Superiore di Sanità.
Ogni centro PMA deve possedere una certificazione di conformità europea (TE), che viene rilasciata dal Centro Nazionale Trapianti (CNT), in collaborazione con le Regioni.
Questa certificazione attesta che il centro è in linea con i requisiti stabiliti dai Decreti Legislativi 191/2007 e 16/2010. Il Centro Nazionale Trapianti organizza con ogni singola Regione un programma di verifica periodica dei centri PMA (cadenza biennale) per certificarne la conformità ai requisiti previsti nei Decreti legislativi. Il programma è iniziato nel 2010 ed è condotto congiuntamente con le Regioni.
Le ispezioni da parte del Centro Nazionale Trapianti (CNT) e delle Regioni sono uno strumento essenziale per garantire che le strutture operino nel rispetto delle normative vigenti in materia di qualità, sicurezza e tracciabilità:
- Ispezioni CNT


Il CNT ha il compito di coordinare, monitorare e vigilare sull’attività dei centri che trattano cellule e tessuti umani, inclusi i centri PMA.
In particolare deve:
- Verificare il rispetto della Direttiva 2004/23/CE e dei decreti attuativi italiani.
- Controllare la qualità e sicurezza nei processi di manipolazione di gameti ed embrioni.
- Verificare la tracciabilità dei materiali biologici.
- Accertarsi della gestione dei rischi e della corretta notifica di reazioni e incidenti avversi.
Gli ispettori del CNT (spesso accompagnati da tecnici regionali) esaminano:
- Documentazione (SOP, registri, certificazioni).
- Locali e attrezzature.
- Conformità dei laboratori (ambiente, temperature, sterili, ecc.).
- Interviste con il personale.
- Ispezioni REGIONALI


Ogni Regione ha il compito di autorizzare, accreditare e vigilare sui centri PMA presenti nel suo territorio avvalendosi del:
- Rispetto delle linee guida nazionali e regionali.
- Controllo delle strutture, del personale e dei protocolli clinici.
- Verifica dell’accreditamento sanitario (presenza di requisiti strutturali, tecnologici e organizzativi minimi).
- Controllo del registro delle attività e degli esiti clinici, da trasmettere annualmente all’ISS.
Durante un’ispezione del CNT o della Regione in un centro PMA, viene effettuato un controllo molto dettagliato relativo al:
1. Laboratorio (embriologia, andrologia, crioconservazione)
- Ambiente controllato: classe di contaminazione, pressione, temperatura, umidità, filtri HEPA.
- Manutenzione e calibrazione di incubatori, cappe, congelatori, centrifughe, ecc.
- Validazione dei processi: vitrificazione, inseminazione, coltura embrionale.
- Tracciabilità dei campioni: etichettatura, registrazione, corrispondenza paziente-campione.
- Gestione della crioconservazione: linea dell’azoto, sicurezza criocontenitori, registro carico/scarico materiale biologico.
2. Documentazione
- Standard Operating Procedures (SOP) aggiornate e approvate.
- Registri di laboratorio e clinici completi e leggibili.
- Moduli di consenso informato, firmati correttamente e aggiornati.
- Registro incidenti/effetti avversi (secondo le direttive europee).
- Documentazione della formazione del personale.
3. Struttura e requisiti organizzativi
- Adeguatezza dei locali: separazione delle aree sterili, percorso pulito/sporco.
- Sicurezza e privacy dei pazienti.
- Organigramma, ruoli e responsabilità ben definiti.
- Presenza di un Responsabile Qualità o equivalente.
4. Personale
- Titoli e competenze del personale (medici, embriologi, personale infermieristico).
- Formazione continua, aggiornamenti professionali, ECM.
- Autorizzazione all’attività sanitaria del personale secondo normativa regionale.
5. Sicurezza e gestione dei rischi
- Procedure per gestione di eventi avversi.
- Piani di emergenza: black-out, guasti tecnici, contaminazioni.
- Sistemi di backup per dati e campioni biologici.
6. Interviste e osservazione
Gli ispettori possono intervistare il personale per verificare conoscenza delle SOP e possono osservare direttamente una procedura simulata o reale (se autorizzata)
7. Indicatori clinici
- Tassi di fecondazione, impianto, gravidanza, nascita.
- Andamento degli esiti clinici rispetto alla media nazionale.
- Compilazione corretta dei dati nel Registro PMA dell’ISS.
Esiti delle ispezioni
- Se tutto è conforme, gli ispettori procedono alla conferma dell’autorizzazione/accreditamento.
- Se emergono non conformità, il centro avrà delle prescrizioni, sospensione temporanea o, in casi gravi, revoca dell’autorizzazione.
- Le non conformità possono essere minori (documentazione, tracciabilità) o maggiori (rischi per la sicurezza dei pazienti o dei materiali biologici).
Conclusioni
Il sistema qualità in un centro PMA è davvero fondamentale perché garantisce che tutti i trattamenti e le procedure siano sicuri, affidabili ed efficaci.
Un sistema qualità ben strutturato assicura che ogni fase, dalla diagnosi alla cura, sia svolta rispettando standard elevati, riducendo al minimo i rischi di errori o complicanze. Inoltre, permette di monitorare costantemente i risultati, migliorare le pratiche e mantenere un alto livello di sicurezza per i pazienti. In sostanza, il sistema qualità aiuta a creare un ambiente di lavoro professionale e trasparente, aumentando la fiducia dei pazienti e assicurando che le tecniche più avanzate siano applicate correttamente. È un elemento chiave per offrire servizi di eccellenza e per il successo dei trattamenti di procreazione medicalmente assistita.


Comments